Absolute Temperatur und thermische Energie
Einer genauere Betrachtung zeigt, dass der über alle Moleküle eines
Systems gebildeten Mittelwert der thermischen Energie ![]() proportional
zur absoluten Temperatur T ist:
proportional
zur absoluten Temperatur T ist:
![]()
Hierbei bezeichnet k die sogenannte Boltzmann'sche Konstante
![]()
Der Proportionalitätsfaktor f , die Anzahl der "Freiheitsgrade", ist eine ganze Zahl und hängt von der molekularen Struktur ab. So ist für einatomige Gase f = 3, für zweiatomige f = 5 (bei hohen Temperaturen auch f = 7) und für Festkörper schließlich f = 6 zu setzen. Bei Flüssigkeiten ist f unbestimmt.
Man sieht aus dieser Beziehung, dass T immer positiv ist, da die mittlere thermische Energie nicht negativ sein kann.
Je höher die Temperatur des Systems, desto heftiger also
ist die Molekülbewegung in seinem Inneren und desto höher die in ihm
"gespeicherte" thermische Energie. Am absoluten Nullpunkt der Temperatur
(T = 0) erstarrt sämtliche thermische Bewegung
(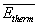 = 0).
= 0).